毎日飲む薬や洗顔後に使う化粧水。それらを手に取るとき、「この製品は安全だ」という前提が、当然のようにそこにあります。でも、その前提はどこから来るのでしょうか?
企業のブランド力による安心感はあると思います。
ですが、その企業が積み上げてきたブランド力の背景には、もう一つ、それを物理的に支える「品質のインフラ」とも呼べる確固たる仕組みが存在しています。
成分表示を確認することはあっても、製品が製造される工程に何重もの管理が組み込まれていることまでを意識する機会は、なかなか無いものです。
GMP(Good Manufacturing Practice:適正製造規範)は、その「見えない安全」を支える製造管理と品質管理の基準です。医薬品・化粧品の製造現場で品質管理・品質保証に関わった経験をもとに、この記事ではGMPの概念から現場での機能のしかた、そして医薬品GMPと化粧品GMPの違いまで、できるだけ具体的に解説します。
業界内の方には改めて整理する機会として、消費者の方には「あの安心」の正体を知る手がかりとして、読んでいただければ幸いです。

GMPとは何か──「いつ、誰が作っても同じ品質」を実現する仕組み
GMPとは、医薬品・化粧品・医療機器・健康食品などの製造において、製品の品質と安全性を確保するための国際的な製造管理基準です。日本語では「適正製造規範」と訳されます。
GMPが目指すのは、一言で言えば「いつ、誰が、どこで製造しても、同じ品質の製品が出来上がること」です。聞くと当たり前のようですが、これを継続的に実現するのは容易ではありません。原材料のロットが変わればわずかに性質が異なることもあり、担当者が変われば手順の解釈にずれが生じることもある。それでも品質を一定に保つために、製造環境・手順・設備・人の動き・記録のすべてを管理するのがGMPです。
GMPが国際的に広まった背景には、歴史的な薬害事件があります。1950年代から60年代にかけて世界各国で問題となったサリドマイド事件は、妊娠中の女性が服用した睡眠薬が胎児の形成に深刻な影響を及ぼした事件で、医薬品の製造管理に対する国際的な意識を根本から変えました。アメリカでは1963年に世界初のGMP規制が連邦規則として施行され、日本では1974年に「医薬品GMP指導基準」が導入されました。以来、科学の進歩や国際的な動向に合わせて繰り返し改訂が重ねられ、現在の医薬品GMPは省令として法的拘束力を持つ基準となっています。
GMPを支える3つの基本原則

GMPは膨大な規定の集合体ですが、その根幹にある考え方は3つに集約されます。現場でGMPを運用するとき、この3つがすべての判断の軸になります。
① ヒューマンエラーを減らす
製造現場では、人間が介在する限りミスは起こりえます。GMPはそれを「個人の注意力に頼る」のではなく、「仕組みとして防ぐ」方向で設計されています。
具体的には、すべての作業をSOP(Standard Operating Procedures:標準作業手順書)として文書化し、担当者がその手順に従って作業することを義務付けます。重要な工程ではダブルチェック(別の担当者による確認)を義務化し、その結果を記録として残します。新しい担当者が配属された際にも、SOPに基づいた教育訓練が完了するまでは単独での作業に就かせないのが原則です。
「この人だから大丈夫」という属人的な安心感ではなく、「この手順に従えば誰でも大丈夫」という状態を作ることを目指しています。
ヒューマンエラーを減らす。言葉にするとすごくシンプルなのですが、これがまた難しいんです。人間がやる以上は、絶対にミスはなくならないんですよね。それを、いかにして仕組み面で減らすかなのですが、結局、仕組みを整えてもそれを動かすのは人間なので、これは永遠のテーマだと思っています。
たとえば、手順書ひとつとっても、文章や写真、図などを用いて作ったりするのですが、人によって解釈の異なる文章ではダメですし、人によって解釈の異なる写真や図でもダメですし。
いざ、手順書が出来上がったら、今度はその内容を教育という形で説明するわけですが、何をもって伝わったか?を判断するのもまた難しい。テストで点数化できれば良いのですが、全部が全部、言語化してテストにできるような内容とは限らない部分もあったり⋯。
仕組みだけでは限界があるし、人間の認知という観点でも限界があるので、最後は両者の絶妙なバランスで成り立っているようなものと言えます。
もう一つ、これは私の体感でしかないのですが、電子化した手順書よりも紙媒体の手順書のほうがミスが少ない印象を受けていました。
紙と画面とで、脳への情報の届き方が異なることを認知科学の観点からまとめた記事も書いています。順序のある内容ほど紙のほうが記憶に残りやすい、という話は手順書にも通じる部分があるかもしれません。

② 汚染と品質低下を防ぐ
製品が外部から汚染されたり、保管中に品質が劣化したりすることを防ぐための管理も、GMPの核心です。
製造現場において特に注意が必要なのが「交差汚染」です。異なる製品の原材料や中間製品が混ざり合うことで、製品の品質が損なわれたり、意図しない成分が混入したりするリスクがあります。これを防ぐために、原材料・中間製品・最終製品・不良品・廃棄物はそれぞれ区別された場所と容器で管理されます。製造エリアへの入退室も管理され、関係者以外は立ち入れないゾーン管理が設けられています。
温度・湿度・空気の清浄度も製品の特性に応じて管理されており、医薬品の注射剤製造などでは清浄度の基準が特に厳格に定められています。
また、製品の性質に応じた適切な容器・包装材料の選定も汚染防止の一部です。光・湿気・酸素などから内容物を守るための包装設計は、品質保持の観点から重要な管理項目となっています。
③ 品質を保証する仕組みを設計する
製造した製品が「たまたま良かった」では品質保証になりません。GMPでは、製造プロセス自体が正しく設計され、意図した結果を確実に生み出すことを科学的に検証する「バリデーション」が求められます。
バリデーションとは、設備・製造工程・分析方法などが規定の条件で確実に機能することを、繰り返し試験・測定によって証明し、文書として記録することです。「これまで問題なかったから大丈夫」という経験則ではなく、データに基づいて有効性を証明することが求められます。一度検証が完了した工程を変更する場合には「変更管理」の手続きが必要になり、事前の評価と承認なしに変更を加えることはできません。また、SOPや規格から外れた事態が発生した場合には「逸脱管理」として記録・原因究明・是正措置が義務付けられます。

医薬品GMPと化粧品GMP──何が同じで、何が違うのか

GMPという言葉は一つですが、医薬品と化粧品では適用される基準の性質が大きく異なります。この違いを理解することは、業界の方が管理の水準を判断する際にも、消費者が製品を選ぶ際にも参考になるかと思います。
医薬品GMP──法律による強制規定
医薬品GMPは、日本では「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律」(薬機法)およびその省令(医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令:GMP省令)に基づく、法的に義務付けられた基準です。この基準を満たさない製造所は、医薬品を製造・販売することができません。
医薬品GMPが特に厳しい理由は、製品が体内に取り込まれるものであり、有効成分の量・純度・安定性が治療効果と安全性に直結するからです。錠剤一錠に含まれる有効成分の量が規定より少なければ治療効果が不十分になり、逆に多ければ過剰摂取のリスクが生じます。このため、原材料の受け入れ検査から製造の各工程での中間品検査、最終製品の出荷前試験まで、すべての段階で試験と記録が求められます。
医薬品GMPでは、「品質管理部門(QC:Quality Control)」と「品質保証部門(QA:Quality Assurance)」が「製造部門」から独立して設置されることが義務付けられています。品質管理部門が試験・検査の実施を担当し、品質保証部門が製造管理・品質管理システム全体の監視と承認を担当します。この独立性は、品質の判断が製造上の都合や生産スケジュールの圧力に左右されないようにするための構造的な仕組みです。製造部門が「今日中に出荷したい」という状況であっても、品質保証部門が不適合と判断すれば出荷は止まります。
また、医薬品の中でも、有効成分(原薬)の製造に特化したGMP基準(ICH Q7:原薬GMPガイドライン)が国際的に定められており、最終製品の品質は原薬の品質に大きく依存するため、原薬の製造工程にも同様に厳格な管理が求められます。
化粧品GMP──国際規格と「任意適用」の実態
化粧品GMPの国際標準として広く参照されているのが、『ISO 22716(化粧品の適正製造基準)』です。これはISO(国際標準化機構)が策定した規格で、2007年に発行され、日本でも日本工業規格(JIS)に対応する規格として採用されています。
医薬品GMPとの最も大きな違いは、日本においてISO 22716の認証取得が「任意」である点です。化粧品の製造は薬機法の規制を受けますが、GMP認証の取得自体は法的義務ではなく、企業が自主的に取り組むものとして位置づけられています。
ただし、これは「化粧品は管理が甘い」ということを意味しません。化粧品も皮膚に直接触れる製品であり、微生物汚染や防腐処方の不備は皮膚トラブルや健康被害につながります。ISO 22716では、原材料管理・製造環境の衛生管理・製造記録・製品試験・苦情対応など、医薬品GMPと共通する多くの管理項目が定められています。
医薬品GMPと比較すると、いくつかの点で管理水準の設計に柔軟性があります。製造設備のバリデーション要件の厳格さ、品質管理部門の独立性に関する規定の詳細度、出荷判定の仕組み、変更管理の手続きの細かさ──これらについては、医薬品GMPほど詳細な要求事項が定められているわけではありません。
これは、化粧品の定義が、「人の身体を清潔にし、美化し、魅力を増し、容貌(ようぼう)を変え、又は皮膚若しくは毛髪を健やかに保つために、身体に塗擦、散布その他これらに類似する方法で使用されることが目的とされている物で、人体に対する作用が緩和なものをいう。(法第二条三項)」とされており、医薬品はピンポイントで特定の症状に効くことを狙うのに対し、化粧品はあくまでも「人の身体を清潔にし、美化し、魅力を増し、容貌を変え、又は皮膚若しくは毛髪を健やかに保つ」こととされているため、副作用面の深刻さという観点からも医薬品ほど厳密に縛られていない部分もあります。
実際に両方の現場を経験して感じるのは、一言で言えば「ガチガチ度合いが違う」ということでしょうか。医薬品の現場では、手順書の一字一句、記録の書き方、判定の根拠まで、すべてに厳密さが求められます。一方で、化粧品の現場では、ある程度の解釈の余地が残されている部分があります。
ただし、それは「管理が甘い」ということではなく、製品の用途とリスクに応じた基準設計の違いと言えます。
とはいえ、両方を知っている立場からすると、その温度差は慣れるまでに少し時間がかかるほど、確かなものとして存在しています。
消費者の視点から見ると、医薬品はGMP省令を遵守することが前提となっているため「GMP認証」などの表現は使いません。それに対し、化粧品の場合、GMPは自主管理基準であるため、企業によってはブランディングや信頼性向上を目的として「GMP認証」を取ることがあります。ただし、その取得状況は企業によって異なりますし、そもそもの前提が化粧品GMPのガイドラインである『ISO 22716(化粧品の適正製造基準)』に則って製造行為が行われるため、認証がないからといって、GMPを満たしていないわけではないのです。
化粧品を選ぶ際にその企業のホームページなどで、「ISO 22716を遵守」とか「GMP基準に基づく製造」といった表記を確認することは、その企業の品質管理への取り組みを知るための一つの判断材料になるかもしれません。
現場でGMPはどのように機能しているのか
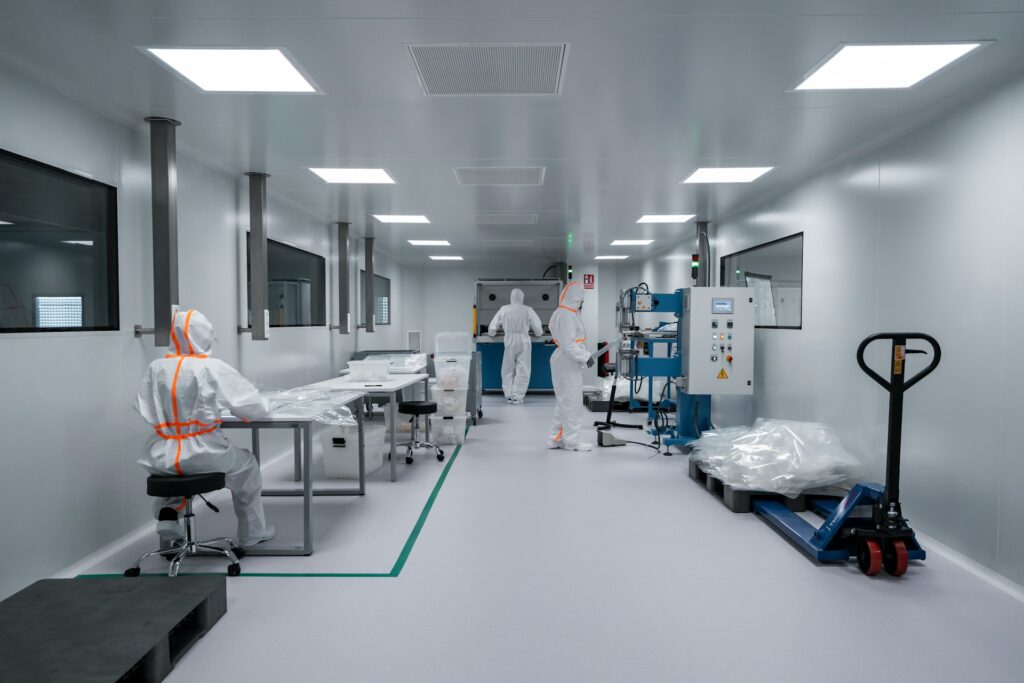
制度としてのGMPと、現場で実際に生きているGMPは、同じものでありながら見える景色が違います。記録、手順書、監査──それぞれが現場でどのような意味を持っているかを、運用の実感から説明します。
SOPという文書の役割──「暗黙知」を「形式知」に変える
SOP(標準作業手順書)は、GMPの現場において最も基本的な文書です。作業の手順を文書化し、誰が担当しても同じ手順で作業できるようにする──それがSOPの目的ですが、その重要性を実感するのはむしろ「人が変わるとき」です。
長年の経験を持つ担当者が退職・異動した際、その人の「やり方」が文書化されていなければ、品質にばらつきが生じるリスクがあります。SOPはそのリスクを抑えるための仕組みで、「この人がいるから安心」ではなく「この手順に従えば安心」という状態を組織として維持することを目指しています。
また、SOPは一度作成すれば終わりではありません。設備の変更・工程の改善・逸脱事例の蓄積などをもとに定期的に見直され、改訂されます。その改訂履歴もすべて記録として残り、「いつ、誰が、なぜ変更したか」が追跡できる状態が維持されます。
医薬品と化粧品の両方で手順書を扱ってみると、その「解釈の余地」の設計そのものが異なることに気づきます。どちらが良い悪いではなく、それぞれの製品特性に応じた合理的な設計の違いです。
記録が持つ意味──追跡可能性という保証
GMP現場で日常的に行われることの一つに、詳細な記録の作成があります。製造記録・試験記録・設備の点検記録・温度湿度の管理記録・従業員の教育訓練記録──これらは単なる書類仕事ではなく、製品の製造履歴を追跡できる「トレーサビリティ」の根拠として機能します。
万が一、製品に問題が発生した場合、記録をもとに「いつ、どの原材料を使って、誰が、どの設備で、どのように製造したか」を追跡することができます。これにより、問題のあるロット(製造単位)を特定し、必要であれば回収の範囲を最小限に絞り込むことが可能になります。
記録の意味を実感したのは、まさしくクレームや問題が発生した場面でした。製造工程に問題がなかったことを記録で示せたこと、原因が製造側にないことを特定できたこと、そして問題のあるとされるロットだけを迅速かつ正確に絞り込めたこと。そして、問題があるとされるロットには異常はなかったこと。記録が正しく残されていたことで、自分たちの潔白を証明することができました。
その時に「もし記録がなかったら⋯」と考えると肝が冷えました。
いくら事実であっても、それを証明できなければ意味がありません。日々の記録業務は、地味で手間のかかる作業に見えますが、問題が起きたその瞬間に、「自分たちを守る証拠」に変わるのです。
また、この記録は消費者を守るための証拠としても機能しています。企業が正しく製造行為を行ったことを証明するものだからです。もちろん、問題が発生した際に、企業が迅速かつ的確に対応するための基盤でもあります。
電子化が進んでいない現場では、この記録が紙で積み上がる量は相当なものになります。保管期間も製品やクライアントによって規定されており、医薬品の製造記録は出荷後一定期間の保存が義務付けられています。
監査という仕組み──外の目が持つ役割
GMP基準の維持には、定期的な「監査」が欠かせません。監査には、社内の担当者が自社の管理状況を確認する「内部監査」と、取引先、行政機関や認証機関が実施する「外部監査(査察)」があります。
内部監査は、日常の運用が基準から外れていないかを定期的に確認し、問題を早期に発見するためのものです。監査結果に基づいて是正措置・予防措置が実施され、その結果も記録として残ります。
外部監査では、審査員や監査員が実際に製造現場に入り、施設の状態・記録の内容・従業員のGMPへの理解度・品質管理システムの機能状況を確認します。医薬品GMPの場合、取り扱う医薬品のリスクに応じて、都道府県や厚生労働省が指定する登録認証機関による定期的な実地調査が行われ、適合していなければ製造許可の維持ができません。外部の視点が入ることで、日常の業務に慣れた内部では見落としやすい点が発見されることもあります。
私がCMO(医薬品製造受託機関)で勤務していた時期、クライアントから顧客査察を受ける経験を何度かしました。毎回感じたのは「指摘のレベル感がクライアントによってまったく異なる」ということでした。同じGMPという言葉を使っていても、どの部分をどの深さで見るかは、クライアントの社内文化や品質への姿勢によって大きく変わります。自社の基準をベースに各クライアントの要求に合わせて対応するのですが、その「合わせる」作業自体に毎回頭を使っていました。
ただ、振り返ってみると、CMOという立場は決して不利なだけではなかったように思います。複数のクライアントと向き合う中で、各社の技術力や品質管理の水準、仕組みや組織風土が自然と見えてくるのです。それは一つのメーカーに勤めていたら得られなかった視点で、技術力も問われる分、自ずと鍛えられる部分も多かったです。
監査の準備は現場にとって相当な業務負荷になることがありますが、それ自体が「記録が整備されているか」「SOPが最新の状態に保たれているか」「教育訓練が実施されているか」を今一度確認する絶好の機会でもあります。
「適合」か「取得」か──制度の違いと維持の重み

医薬品はGMP省令を遵守することが求められるため、GMPは義務です。そのため、GMPの認定を取得するとは表記しません。あくまでも、「適合」か「不適合」となります。
一方で、化粧品においてGMPは自主的な取り組み(任意)であるため、あえて「取得」と表記することで、その企業の品質へのこだわりを可視化しているという側面があります。
医薬品GMPは「適合の維持」
医薬品GMPの場合は、先ほども少し触れましたが、取り扱う医薬品のリスクに応じて都道府県や厚生労働省が指定する登録認証機関(PMDA)が審査を行います。申請書類の提出から始まり、書面審査・実地調査・審査会での審議を経て、適合していれば認定が通知されます。結果が出るまでには通常6ヶ月から1年程度の期間を要し、日本では3年ごとに更新審査が必要です。
少し複雑化してしまうので整理しておきます。
ここで触れているのはGMPの「適合性調査」になります。医薬品を作る行為の許認可である「製造業許可」は5年ごとの更新になるのですが、その間にGMP管理が適切になされているかをチェックする「適合性調査」が3年ごとにあります。
書面審査では、品質管理システムがGMP基準に適合しているか、SOPが適切に整備されているか、記録の管理体制が確立されているかが確認されます。書面審査を通過すると、審査員が実際の製造現場を訪問し、書類と現場の実態が一致しているかを確認します。施設の状態・設備の管理状況・従業員のGMPへの理解度・記録の信頼性・品質管理部門の機能などが検証の対象になります。
化粧品GMPは「認定の取得」
化粧品GMPの場合は、民間の第三者認証機関が審査・認証を行います。
基本的な審査の構造は同様ですが、強制力や審査の厳格さは医薬品GMPとは異なります。
重要なのは、認定を一度取得すれば終わりではない点です。GMP認定はその時点での管理状況の証明であり、その後も継続的な維持が求められます。記録の管理・定期的な内部監査・従業員教育の継続・設備の定期点検──これらが途絶えれば、次の更新審査で問題が生じます。
消費者が「GMP認証」という表記を目にした際には、どの機関・基準に基づく認証なのかを確認することも参考になります。
あの安心は、こうして作られている

薬を飲むとき、化粧品を使うとき、多くの人はその製品が安全であることを前提にしています。その前提を支えているのが、GMPという製造管理と品質管理の仕組みです。
原材料が届いてから試験・確認され、適切な環境で保管され、文書化された手順に従って製造され、中間品が検査され、包装され、最終製品として出荷前試験に合格して初めて市場に出る。その一連の過程がすべて記録され、逸脱があれば報告・是正され、定期的に内部・外部の両面から正しく行われているかを確認される。そういう積み重ねが、製品棚に並ぶ一本の化粧水や一錠の錠剤の背景にあります。
「安全は一度確保すれば終わり」ではなく、「安全は維持し続けることで成り立つ」という考え方が、GMPの根底にあります。それは完璧なシステムを作って終わりではなく、常に問題が起きないように、また、たとえ問題が起こってしまっても速やかに発見し、修正できる仕組みを継続的に機能させ続けることを意味しています。
製品を手に取るとき、その背景にこうした仕組みがあることを知っておくことは、消費者として製品を選ぶ視点を少し変えてくれるかもしれません。そして製造に関わる方には、日々の記録や手順書の維持が持つ意味を、改めて確認する機会になれば幸いです。


.webp)






